Portaalsite voor de échte zeeaquariaan
De Wodka-methode - Bestrijding van nitraat- en fosfaat-overschotten in het zeeaquarium – versie 2014
Algenontwikkeling, bruinkleuring van kortpoliepige steenkoralen, achterblijvende groei, dagelijkse aanslag op de ruiten - veelgehoorde en regelmatig terugkerende problemen. Sommige ervan horen bij de opstart- of doorstartfase, andere horen bij de wat verder gevorderde bakken waarin met name de aquariaan zijn gevoel voor evenwicht kwijt is. De problemen kennen meerdere oorzaken en zijn in beginsel eenvoudig aan de bron aan te pakken. Het doseren van een koolstofbron (wodka-methode, VSV-methode en alle commerciële nitraatverwijderaars) is slechts een lapmiddel, maar kan, mits het systeem in evenwicht verkeert een toegevoegde waarde leveren aan de kwaliteit van het aquarium.
1. Waar komen nitraat en fosfaat vandaan, waarom hopen ze op en welke problemen brengen ze met zich mee?
De werking en regeneratie van het fosfaatfilter.
Inleiding
Veel aquarianen hebben tegenwoordig een fosfaatfilter in het aquarium/sump om het fosfaat gehalte in het water zo laag mogelijk te houden. Dit is vooral gekomen met de grote aandacht voor LPS koralen, zoals Acropora’s. Een laag fosfaatgehalte (<0.03 ppm PO4) is noodzakelijk om steenkoralen goed te laten groeien. Als het fosfaatgehalte boven de 0.05 ppm komt zal de koraalgroei ernstig geremd worden, omdat er zich dan een fosfaat laagje op de koralen afzet en daar wordt moeilijk calciumcarbonaat op afgezet.
Een tweede negatief gevolg van te hoog fosfaatgehalte is te veel algengroei. De groei van algen is grofweg evenredig met de fosfaat concentratie. Om de algengroei dus te beheersen is een laag fosfaat gehalte wenselijk.
Fosfaat wordt in het aquarium o.a. verwijderd door middel van biologische afbraak door bacteriën, opname door koralen, opname door macroalgen/wieren of de eiwitafschuimer. Als er echter zoveel gevoerd wordt dat de natuurlijke opname/afbraak van fosfaat niet snel genoeg gaat, dan moet er ingegrepen worden om te voorkomen dat het fosfaat gehalte boven de 0.05 ppm stijgt.
Een van de meestgebruikte oplossingen is het installeren van een fosfaatfilter. Dit is meestal een vat/reactor waar het filtermateriaal ingaat, een pomp die daar op wordt aangesloten zorgt voor de watercirculatie.
Een beetje filterwatten onder en boven het filtermateriaal zorgt ervoor dat dit in de reactor blijft en niet in het aquarium terecht komt. Het filtermateriaal eerst goed onder de kraan uitspoelen om kleine stofdeeltjes te verwijderen.
Filtermaterialen
Nu eerst even iets over de verschillende filtermaterialen.
De huidige fosfaatadsorptie materialen bestaan vooral uit een poreus ijzerhydroxide (Fe(OH)3), wat als een delfstof gewonnen wordt. Het is te herkennen aan de roestbruine kleur. Voorheen werd er ook aluminiumoxide als fosfaatadsorptie middel gebruikt, dit is te herkennen aan de grijs/witte kleur.
In dit artikel zal ik verder ingaan op de ijzerhydroxide fosfaatadsorptie materialen, in de aquariumhandel te verkrijgen als: o.a. Phosban, Phosfate killer en Rowaphos .
In het promotie onderzoek van Alexander Sperlich (Berlijn, 2010) 1) is heel veel informatie te vinden over het gebruik van ijzerhydroxides als fosfaatadsorptie middel in afvalwater. Nu is ons aquariumwater wel geen afvalwater, maar het doel is hetzelfde: fosfaat uit water verwijderen.
Zoals gezegd is ijzerhydroxide een poreus mineraal. Het is zo poreus, dat de kleine kanaaltjes in dit materiaal een oppervlak hebben van ca. 250 m2/g. Fosfaat in het water zal zich zowel aan de buitenkant van de korrels als in de poriën aan het ijzerhydroxide hechten. Om goed gebruik te maken van het oppervlak in die poriën moet het water er natuurlijk wel doorheen stromen. Dit gaat niet zomaar, omdat die poriën heel erg klein zijn. Vandaar dat ik aanraad het adsorptie materiaal op te sluiten in een reactor en daar water doorheen te pompen. Op die manier zal het water ook in de poriën dringen en niet alleen langs en over de korrels lopen.
Dit geldt natuurlijk ook voor een actieve kool filter!!
Het adsorberen van fosfaat aan ijzerhydroxide is een relatief langzaam proces. Als men te hard pompt zal het fosfaat niet voldoende gelegenheid krijgen te hechten aan het ijzerhydroxide en gewoon door het filter lopen. Het water moet zodanig hard door het filter lopen dat de stroomsnelheid 1/3 van het volume per uur is. Ter verduidelijking: met 1 liter filtermateriaal moet men ongeveer 330 ml/uur water pompen.
De reden dat het water door de korrels en poriën moet lopen is tegelijk het argument tegen het gebruik van wervelbed filters als fosfaatfilter. Het water zal dan voornamelijk langs de korrels lopen en niet er door heen, zodoende wordt er geen gebruik gemaakt van het inwendig oppervlak van de korrels en wordt de maximale capaciteit van de korrels niet gebruikt.
Opname capaciteit.
Hoeveel fosfaat kan er nu eigenlijk opgenomen worden door de ijzerhydroxide korrels?
Die opname is o.a afhankelijk van de pH van het water en van de aanwezigheid van calcium. Bij hogere pH zal er minder fosfaat opgenomen worden dan bij lagere pH, bij aanwezigheid van calcium zal er echter weer meer fosfaat opgenomen kunnen worden. Voor toepassing in een zeewateraquarium hebben we wat dat betreft niet zoveel te kiezen en lijken deze effecten elkaar op te heffen.
Volgens de studie van Sperlich 1) kan er theoretisch 23.6 mg P per gram ijzerhydroxide opgenomen worden. In testen hebben zij echter gevonden dat er respectievelijk 39.5 en 51.9 mg P/g ijzerhydroxide opgenomen is, o.a afhankelijk van het water dat ze gebruiken.
Wat betekent dit voor ons aquariumhouders?
Stel, we hebben een aquarium van 1000 liter zonder fosfaat filter en het water bevat 0.5 ppm fosfaat. Hoeveel fosfaatkiller hebben we dan nodig om dit te verwijderen? We nemen aan dat er even geen fosfaat gevormd wordt.
In het water zit 0.5 ppm fosfaat, dit is voor het hele aquarium 0.5 x 10-6 x 1000 x 1000 gram= 0.5 gram (=500 mg) fosfaat. Een gram fosfaatkiller kan ongeveer 25 mg (minimaal) fosfaat opnemen, je hebt dan 500/25 = 20 gram fosfaatkiller nodig om alle fosfaat uit het water te halen. Waarschijnlijk is dit een minimale hoeveelheid fosfaat-adsorber, afhankelijk van het type/merk zal er meer of minder fosfaat geadsorbeerd worden. Het geeft in ieder geval wel een goede indicatie hoeveel fosfaat killer je nodig hebt. Na verloop van tijd zal het fosfaat filter natuurlijk verzadigd zijn. Dit zou je kunnen testen door het water dat uit het filter loopt te vergelijken met het water in het aquarium. Is het fosfaat gehalte gelijk, dan is het filter verzadigd en moet je het verwisselen of regenereren.
Regeneratie
Ja, regenereren is ook mogelijk!!
Omdat het adsorptie vermogen pH afhankelijk is, is het mogelijk bij hoge pH het fosfaat weer weg te spoelen.
Een goede methode is beschreven in de artikelen van Matt Wandell en Laura Kormos in AdvancedAquarist 2) en van Sperlich 1).
Verwijder eerst het fosfaat filter uit het aquarium of sump.
Maak een oplossing van 40 gram NaOH (gootsteenontstopper) /liter water. Let wel op!!! Deze vloeistof is erg agressief, bijtend. Gebruik handschoenen als je hier mee werkt!!
Neem hiervan minimaal 4-6 keer het volume van het fosfaatadsorptiemiddel en pomp dit enige uren rond (bij voorkeur in je fosfaatfilter). Het desorberen van fosfaat gaat veel sneller in vergelijking met het adsorberen en kan daarom met grotere pompsnelheid en in minder tijd gebeuren.
Daarna enige tijd met water spoelen, niet rondpompen maar het water uit het filter weg laten lopen, tot het water neutraal is. Alle loog en fosfaat zullen dan weg zijn. Het blijkt dat het fosfaatfilter dan voor 80% zijn capaciteit weer terug heeft.
Soms is de inhoud van het fosfaat filter tot een of enkele grote stukken samengeklonterd. Dit wordt meestal veroorzaakt door kalkafzetting op het ijzerhydroxide. Je kunt dit controleren door een stukje af te breken en dit in wat schoonmaakazijn of verdund zoutzuur te leggen. Als er kleine gasbelletjes ontstaan is dit het bewijs dat er kalk aanwezig is. Voor de regeneratie met loog te starten, kan je nu beter eerst met verdund zoutzuur spoelen om eerst al het kalk te verwijderen zodat het ijzerhydroxide weer als losse korrels in het filter zit. Daarna kan je de regeneratie met loog starten.
De afzetting van kalk wordt veroorzaakt door de plaatselijke hoge pH aan het oppervlak van het ijzerhydroxide 3). Het oppervlak van het ijzerhydroxide bevat veel OH- groepen (fig. 1). Als er fosfaat geadsorbeerd (fig.2) wordt zullen deze OH- groepen vrij komen en aan het oppervlak voor een stijging van de pH zorgen. Als de pH stijgt zal de oplosbaarheid van kalk afnemen en dus neerslaan op het ijzerhydroxide. Dit zorgt op den duur voor het samenklonteren van het ijzerhydroxide.
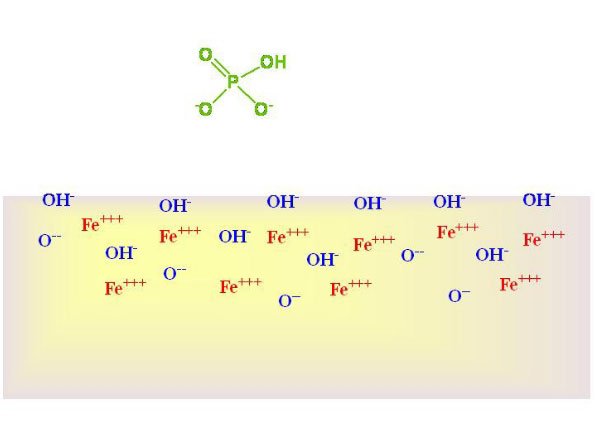
Fig. 1. Fosfaat (in de meest voorkomende vorm in zeewater, HPO4- -) boven een ijzerhydroxide oppervlak.
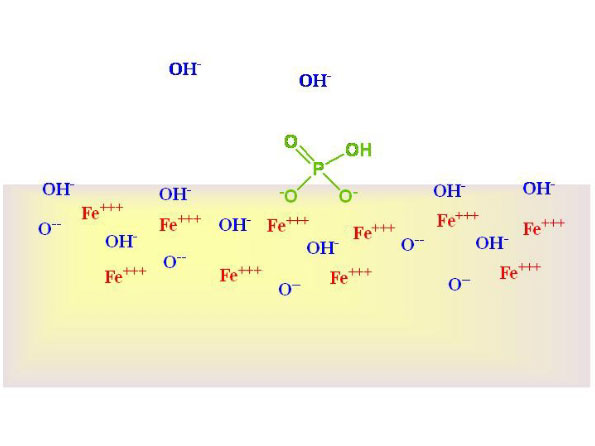
Fig. 2 Fosfaat dat hydroxide (OH-) verdringt en aan het ijzerhydroxide oppervlak bindt.
Nadelen.
Natuurlijk zijn er ook (mogelijke) nadelen aan het gebruik van fosfaat adsorbers. Zoals bijna alle adsorbers, zijn ze niet specifiek voor één stof, er zullen ook andere stoffen geadsorbeerd worden. IJzerhydroxide is vooral bekend om de adsorptie van arseen. Maar het is te verwachten dat ook diverse andere spore elementen als silicium, mangaan, kobalt, nikkel, en zink door het ijzerhydroxide geadsorbeerd worden. Ook organische fosfaten kunnen door het fosfaatfilter opgenomen worden. Fosfaat filters kunnen vooral polaire hydrofiele stoffen adsorberen, terwijl apolaire stoffen juist door actieve kool geadsorbeerd wordt. Fosfaatfilters en actieve kool filters zijn dus complementair.
Als je voor het eerst een fosfaatfilter gaat gebruiken, omdat het fosfaat gehalte te ver is opgelopen, ben je natuurlijk genegen om dit zo snel mogelijk omlaag te krijgen. Dat is misschien niet de juiste manier, het is beter om het fosfaat gehalte geleidelijk omlaag te brengen, om zodoende een schokeffect voor de koralen, door te snelle fosfaat daling, te voorkomen.
Zoals al eerder gezegd belemmert een hoog fosfaatgehalte de koraalgroei. Als er echter te weinig fosfaat aanwezig is, zullen de koralen ook niet meer groeien. Denk hier aan als je een aquarium hebt met veel steenkoralen, die fosfaat gebruiken voor de groei, en een fosfaatfilter met grote capaciteit. Het kan dan nodig zijn het fosfaat filter enige tijd uit te zetten.
Referenties
1) Phosphate adsorption onto granular ferric hydroxide (GFH) for waste water reuse, by Alexander Sperlich.
https://depositonce.tu-berlin.de/handle/11303/2870
2) Regeneration of granular Ferric Oxide Media with Sodium Hydroxide, by Matt Wandell, Laura Kormos
3) Iron Oxide Hydroxide (GFO) Phosphate binders, by Randy Holmes-Farley
http://reefkeeping.com/issues/2004-11/rhf/index.php
Ongewone sporenelementen: IJzer.
IJzer is een scheikundig element met symbool Fe (uit het Latijn: ferrum) en atoomnummer 26. Het is een grijs overgangsmetaal. In de volksmond wordt de term ijzer vaak gebruikt voor materiaal dat eigenlijk staal heet. Uit opgravingen blijkt dat rond 4000 v.Chr. ijzer al werd gebruikt in Sumer en het Oude Egypte voor speerpunten en ornamenten. Veelal was het ijzer hiervoor afkomstig van ingeslagen meteorieten (het zogenaamde meteoorijzer) In de daarop volgende eeuwen werd het gebruik van ijzer verspreid naar Mesopotamië, Anatolië, Midden-Oosten en andere gebieden. Nadat men ontdekte hoe men ijzer uit zijn ertsen kon winnen en vervolgens smeden, nam het gebruik een grote vlucht. Tussen de 12e eeuw v.Chr. en de 10e eeuw v.Chr. nam ijzer de plaats van brons over bij de productie van gereedschappen en wapens. Deze overgang van brons naar ijzer, die de ijzertijd inluidde, werd niet zozeer veroorzaakt door betere eigenschappen van ijzer, maar meer door sterk geslonken beschikbaarheid van tin, een hoofdbestanddeel van brons. In het Midden-Oosten ontdekte men dat de kwaliteit kon worden verbeterd door het ruwe ijzererts te verhitten in een bed van houtskool. Later werd dit procedé bekend als carbonisatie. In China werd het principe van de hoogoven bedacht en kon de kwaliteit van het ijzer verder worden verbeterd. Er kwam dan meer koolstof in het ijzer waardoor ze al een soort staal kregen, een legering van ijzer en koolstof. De naam ijzer is afkomstig van het Oergermaanse woord īsarna-, wat op zijn beurt mogelijk weer afkomstig is van het Proto-Indo-Europees is-əro- "sterk (metaal, in vergelijking met het zachtere brons)". IJzer heeft door de eeuwen heen al altijd een belangrijke rol gespeeld. Maar ook in de biologie, en met name in de oceaan, heeft ijzer een relatief groot aandeel. Al wat in de oceaan afspeelt, speelt zich ook af in ons aquarium. Daarom wat meer over ijzer.
IJzer algemeen
Archeologisch bewijs toont aan dat mensen ijzer al minstens 5000 jaar gebruiken. IJzer is het goedkoopste metaal en een van de meest voorkomende metalen, omdat bijna 5,6% van de aardkorst en bijna de gehele aardkern bestaat uit ijzer. IJzer wordt met name gewonnen uit de mineralen hematiet (Fe2O3) en magnetiet (Fe3O4). De mineralen taconiet, limoniet (FeO(OH)·nH2O) en sideriet (FeCO3) zijn andere belangrijke ijzerbronnen. IJzer is een zeer nuttig element, omdat het behalve bij de opbouw van de aarde ook een rol speelt bij het in leven houden van planten en dieren. IJzer speelt een rol in de fotosynthese van planten (zoöxanthellen) en het is een essentieel onderdeel van hemoglobine, de rode bloedkleurstof die zuurstof door het lichaam vervoert. IJzer- sulfaat (FeSO4) wordt bijvoorbeeld gebruikt om bloedarmoede te behandelen.
Alle levende wezens hebben ijzer nodig. Sommige krijgen het met voedsel binnen, anderen door opgelost ijzer te absorberen. In vele natuurlijke omgevingen, variërend van delen van de oceaan tot het menselijk lichaam, kan ijzertekort de reden zijn dat de groei stagneert, ijzer is dan de beperkende factor in het voedsel. Het feit dat de meeste organismes slimme methoden hebben ontwikkeld om ijzer uit hun omgeving te halen geeft wel aan dat ijzer erg belangrijk voor ze is. Maar waarom? Het blijkt dat ijzer, ontelbare toepassingen heeft in biologische systemen. Een heel bekende is dat ijzer een belangrijk bestanddeel is van hemoglobine. IJzer zorgt ervoor dat hemoglobine zuurstof kan binden en zodoende door het lichaam kan transporteren. Vissen hebben grote hoeveelheden hemoglobine in hun bloed en zijn zo in staat heel efficiënt zuurstof van de kieuwen naar de rest van het lichaam te transporteren. Vissen krijgen hun ijzer uit voedsel, en zolang ze dus goed gevoerd worden krijgen ze geen ijzertekort, ongeacht de concentratie ijzer in het water.
IJzer komt in twee ionvormen voor, Fe2+ en Fe3+. Dit komt bij niet veel metalen voor, en daarom kunnen organismen ijzer gebruiken op een manier die niet mogelijk is bij andere metalen. IJzer wordt daarom in feite door alle organismen in heel veel proteïnen en andere typen organische moleculen gebruikt. Veel van deze toepassingen maken gebruik van de heen of teruggaande redoxreactie tussen de twee vormen van ijzer: Fe++àß e-+Fe+++
Terwijl ijzer nog in puur water, nog aan droge lucht duidelijk verandert, gaat het bij aanwezigheid van water en zuurstof, dus bijvoorbeeld aan vochtige lucht, roesten. De zilverige kleur verandert hierbij in bruinrood, omdat het gehydreerde oxide gevormd wordt. In het water opgeloste elektrolyten versnellen de reactie die eruitziet als volgt:
4Fe + 3O2 + 6 H2O -> 4Fe3+ + 12(OH)- -> 4Fe(OH)3 of 4FeO(OH) + 4 H2O
Meestal beschermt de gevormde roestlaag het ijzer niet voor een verdere reactie, maar valt af, zo dat meer metaal kan oxideren. Bij de aanwezige elektrolyten gaat het voor een groot deel om ijzer(II)sulfaat (FeSO4) dat bij aanval door atmosferisch Zwaveldioxide (SO2)ontstaat. In regio’s die vlakbij de zee liggen, spelen ook zoutdeeltjes in de lucht een belangrijke rol.
IJzer(III)hydroxide (4Fe(OH)3 ) slaat ook in natuurlijke wateren vaak neer.
IJzer vs fotosynthese
Onze koralen, doopvontschelpen en algen doen allemaal aan fotosynthese. Om dit proces uit te kunnen oefenen hebben ze allemaal speciale symbiotische cellen die chloroplasten bevatten. In het chloroplast vindt de fotosynthese plaats. De vloeistof die de rest van de chloroplast opvult heet het stroma. Daarnaast zitten er nog zetmeelkorrels in de chloroplast. De chloroplasten bevatten op hun beurt weer thylakoïden. Een thylakoïde is een aan het fosfolipidedimembraan gebonden compartiment in de chloroplasten en cyanobacteriën. Ze bestaan uit een thylakoïde membraan rond een thylakoïde lumen .Thylakoïden bevatten veel integrale membraaneiwitten, die belangrijk zijn voor de fotosynthese. De membranen van de thylakoïden bevatten chlorofyl en enzymen die nodig zijn voor de lichtreacties van de fotosynthese. Thylakoïden in chloroplasten vormen stapels, die grana (enkelvoud: granum) worden genoemd. Dit is door veel aquarianen reeds bekend. Wat onbekend is dat ze naast chlorofyl ook een cytochroom bevatten. Chlorofyl en cytochroom lijken qua bouw heel veel op elkaar. Beide moleculen hebben een ringvormige structuur. Echter, in het chlorofyl zit in het centrum een magnesiumatoom, terwijl er in het cytochroom een ijzeratoom zit. Een ander bekend molecuul dat heel sterk lijkt op het cytochroom is hemoglobine dat de zuurstof in ons bloed bindt en eveneens een ijzeratoom bevat. Dat cytochroom is belangrijk in het doorgeven van de opgevangen energie uit licht aan andere moleculen. We weten inmiddels dat ijzer in verschillende vormen (Fe2+ en Fe3+) kan voorkomen. Nu komt het vervelende. In het hart van het cytochroom moet een Fe2+. Een Fe3+ past niet! Geen probleem, dan neemt de plant maar een Fe2+ op, zou u misschien denken. Maar Fe2+ is een lastpak. Zo gauw als het de kans krijgt wil het Fe3+ worden. Licht en zuurstof bijvoorbeeld zijn al voldoende om het Fe2+ om te laten zetten in Fe3+. Dus als u een ijzersupplement koopt in de winkel zit daar een chelaat (Meestal EDTA) bij. Dat chelaat is een fraai molecuul meestal in de vorm van een grote C. Twee van de moleculen kunnen zo een Fe2+ omklemmen zodat er niets mee kan gebeuren. Alleen de cytochromen kunnen het ijzer er weer uit halen. Alleen bij een goede ijzerbevoorrading zal het cytochroom dus goed functioneren. Wanneer dit niet het geval is krijgen we een onbalans zodoende dat de chloroplast langzaam zal aftakelen. We kunnen echter niet zonder deze organellen daar ze instaan voor de voeding van de symbiosepartners. Bij het bleachen door warmte is het ook het cytochroom dat door de warmte als eerste afsterft waardoor de symbiotische cel afsterft en wordt losgelaten.
Samengevat:
Onze koralen bevatten zoöxanthellen of symbiotische algen. Deze bevatten net zoals alle andere cellen organellen zoals een kern, een membraan maar ook een chloroplast. Deze wordt in de volksmond ook wel eens bladgroenkorrel genoemd. In deze chloroplast vinden we structuren terug die wat weg hebben van kleine flatgebouwtorens. Deze torens die ook wel granum genoemd worden bestaan vervolgens uit vele kleine kamertjes die samen de toren vormen. Deze kamertjes (appartementjes op zich zelf) noemen we de Thylakoïden. De bakstenen en muren waar de appartementjes uit opgebouwd zijn bestaan deels uit het chlorofyl en cytochroom. Deze laatste twee staan in voor het opvangen van licht en het transporteren van het voedsel, dat gemaakt is uit het licht.
Het cytochroom is een ringvormig molecuul met in het hart een tweewaardig ijzeratoom (Fe2+). Cytochroom is onontbeerlijk voor de fotosynthese.
IJzer in zeewater
IJzer in de oceaan is voornamelijk ijzer(III) (Fe3+), omdat alle Fe2+ dat gevormd door zuurstof en andere oxiderende stoffen teruggeoxideerd wordt tot Fe3+. De ijzerconcentratie varieert behoorlijk per locatie en diepte, en wordt aan de oppervlakte minder door opname van organismen (micro-algen). Typische oppervlakteconcentraties zijn in de orde van 0,000006 ppm (70 pmol/kg). De gemiddelde concentratie is 540 pmol/kg. Als ijzer niet gebonden is aan een organisch molecuul, bestaat ijzer in zeewater vooral als opgelost IJzer(III)oxide (Fe(OH)3). IJzer(III) is overigens behoorlijk onoplosbaar in zeewater bij een gemiddelde pH 8,2 vanwege de vorming van verschillende vormen ijzeroxide(roest). In feite, is het een van de slechtst oplosbare kationen in zeewater. Dus, een grote hoeveelheid ongebonden ijzer een aquarium ingooien zal alleen uitdraaien in het neerslaan op de bodem. In de meeste oceanen wordt de groei van micro-algen beperkt door stikstofbronnen (nitraten). In sommige plaatsen echter, waar genoeg stikstof, fosfor, en silicaat (diatomeeën) aanwezig is, wordt de groei van micro-algen beperkt door de beschikbaarheid van ijzer. Experimenten in de oceaan hebben aangetoond dat de groei kan worden versneld door het toevoegen van ijzer. Tevens hebben experimenten in de oceaan aangetoond dat na het toevoegen van ijzer vooral de diatomeeën, cyanobacteriën en dinoflagellaten het hardst groeien. De ratio die gekend is tussen ijzer en fosfor bedraagt gemiddeld 1:100.
|
Zeewater |
1-3 ppb of 0.003 ppm |
|
Rivierwater |
0.5-1 ppm |
|
Algen (flagellaten) |
20-200 ppm |
|
Bruinalgen |
4000 ppm |
|
Schelpdier |
195 ppm |
|
zeewatervis |
10-90 ppm |
Gemiddelde waarde in vergelijking tot elkaar. Deze zijn gebaseerd op drogestofgehalten. Verbazingwekkend is dat de bioconcentratiefactor van algen tot zeewater maar liefst 104-105 bedraagt.
IJzer als wereldredder?
We weten inmiddels dat ijzer een belangrijk element is voor de fotosynthese en gezonde algen. Gezonde algen zullen zich ook voortplanten en daar hebben enkele wetenschappers het ei van Columbus gevonden, althans dat dachten ze. Het begon toen Australische wetenschappers hebben ontdekt dat de uitwerpselen van walvissen een belangrijke rol kunnen spelen in het reduceren van de hoeveelheid koolstofdioxide (CO2) in de atmosfeer. De ijzerrijke uitwerpselen zorgen ervoor dat algen groeien. En voor die groei is veel koolstofdioxide (CO2) nodig. De onderzoekers analyseerden de uitwerpselen van de walvis en ontdekten dat deze tien miljoen keer meer ijzer bevatten dan zeewater. De wetenschappers ontdekten dat de hoeveelheid ijzer, wanneer krill algen eten en walvissen vervolgens deze krill eten, toeneemt. En dat is goed nieuws voor het klimaat, zo concludeert onderzoeker Andrew Bowie. “Wanneer algen groeien ondergaan ze het proces van fotosynthese en voor een deel van dat proces wordt koolstofdioxide (CO2) uit de atmosfeer onttrokken.” Meer walvissen zou dan ook meer algen en dus minder koolstofdioxide betekenen, zo concluderen de onderzoekers. Nog een reden om walvisvangst te stoppen! Maar toen kwam het idee pas echt tevoorschijn. Niet veel later besloten enkele andere wetenschappers om tonnen ijzer in de oceaan te gooien en te onderzoeken hoe de algengroei op gang kwam en voorral, hoe de algen vervolgens koolstofdioxide (CO2) zouden gaan opnemen. Het broeikasprobleem was zo opgelost, de algen zouden het werk gaan doen. Ze vergaten echter dat er meer bij kwam kijken. Er was namelijk één algsoort die enorm goed reageerde op het ijzer en welke ook met kop en schouders boven de rest uitstak qua groei en aantal. De algen die domineerden waren van het Pseudonitzschia-geslacht en produceren een grote hoeveelheid domoïne-zuur ((2S,3S,4S)-4-[(2Z,4E)-6-carboxyhepta-2,4-dien-2-yl]-3-(carboxymethyl)pyrrolidine-2-carboxylzuur, C15H21NO6). Dit neurotoxine bindt zich aan de glutamaatreceptoren van neuronen en veroorzaakt daardoor geheugenverlies, verward gedrag, en in ernstige gevallen een dodelijke hersenbeschadiging. Dit zuur is een neurotoxine (zenuwgif). De concentraties domoïne-zuur in de oceaan stijgt drastisch als de bepaalde algensoort ‘bloeit’ op zijn natuurlijke tijden. De concentratie na de proeven was onmenselijk groot! Gelukkig werden de wetenschappers teruggefloten door vele andere wetenschappers. Het is echter niet onvermijdelijk, maar de bloei van Pseudonitzschia kan ook natuurlijk voorkomen. Dit heeft soms grote gevolgen voor het gehele ecosysteem.
Domoïne-zuur doodt soms dieren, zoals zeeleeuwen. Stel, grote hoeveelheden ansjovis zijn besmet met het gif, dan is het eten van ansjovis voor zeeleeuwen, pelikanen of zeevogels voldoende om te sterven. Vaak gaat vergiftiging gepaard met agressiviteit. Er zijn gevallen bekend van getroffen zeeleeuwen die mensen aanvielen. Dit o.a. in Californië waar zeeleeuwen massaal gaan uitrusten op boten in havens. Ook het stadje Capitola in de Verenigde Staten werd in 1961 aangevallen door groepen zeevogels, die mogelijk onder invloed waren van het zenuwgif. Een incident waardoor Alfred Hitchcock werd geïnspireerd om de beroemde film ‘The Birds’ te maken. Daar blijft het echter niet bij. Iedereen weet dat de mosselen uit de rekken gehaald kunnen worden, ook deze schelpdieren kunnen deze algen gegeten hebben en vervolgens het Domoïne-zuur bevatten. Het eten van mosselen met dit vergif zou niet verstandig zijn en zou lijden tot ASP (Amnesic shellfish poisoning). Hier komt dan weer de spreuk vandaan: “in de maanden met een ‘R‘ eet je de mosselen her en der”. Dit komt omdat in de maanden waar geen ‘R’ in voorkomt vaak de bloei voorkomt. Nu heeft de mosselindustrie dit aardig onder controle zodat er steeds mosselen beschikbaar zijn.
Waarschijnlijk is het nog te vroeg om ijzerbemesting aan te dragen als een manier om het broeikaseffect tegen te gaan. Eerst moeten wetenschappers meer te weten komen over de effecten en gevolgen van het uitzetten van ijzer. Ook moeten ze vragen stellen zoals: In welke situaties wordt domoïne-zuur geproduceerd? En is er misschien een manier om koolstofdioxide (CO2) op te slaan in de oceanen, zonder dat het gif wordt aangemaakt door algen? Ook ureum ((NH2)2CO) (wordt vaak als meststof bij algenkweken gebruikt) staat bekend om in combinatie met hoge nitraatwaarden algen aan te zetten tot de vorming van domoïne-zuur.
IJzerbehoefte in ons aquarium
Het toevoegen van ijzer heeft een aantal voordelen. Ten eerste kunnen bepaalde macro-algen sneller groeien en er donkerder, mooier groen uitzien als er ijzer aan het aquarium wordt toegevoegd. Macro-algen zijn algen die met het blote oog zichtbaar zijn, kleinere algen die alleen met de microscoop te zien zijn heten micro-algen. Bovenop dit esthetische voordeel, zorgt deze toegenomen groei ervoor dat de macro-algen een beter nutriëntexportsysteem zijn. Een ander voordeel is dat snel groeiende macro-algen beter concurreren met micro-algen, die vaak een bron van frustratie zijn voor aquarianen. Ook kunnen sommige algen en bepaalde bacteriën organische stoffen afscheiden die mogelijk aanwezige ijzer(III)oxide ((Fe2O3) zullen doen oplossen. Dit doen ze omdat dit vervolgens voor hun weer opneembaar wordt.
Ten tweede is men er van overtuigd dat ijzer belangrijk is voor groenkleuring bij koralen. Dit komt deels door de cytochromen. Bij een juiste verhouding ijzer zullen de cytochromen zich groter maken. Samen met het chlorofylgehalte zorgt lichtweerkaatsing voor de optisch groene kleur. Er zijn natuurlijk meer factoren die belangrijk zijn voor het in stand houden van de mooie kleuren van koralen. De soort en hoeveelheid licht, de pH, de alkaliniteit, de hoeveelheid nutriënten, sporenelementen (ook ijzer), bacteriën en aminozuren zijn allemaal belangrijk voor de kleuring van de koralen. Als een van deze factoren niet geheel goed is zullen de kleuren niet optimaal zijn. Verwacht dus niet alles van een ijzer toevoeging. Daarnaast is een goed ijzergehalte belangrijk om de fotosynthese processen uit te voeren. Onze koralen maar ook doopvontschelpen doen aan fotosynthese waardoor ijzer een belangrijk element is. Als laatste hebben ook onze vissen een behoefte aan ijzer. Zij nemen dit op uit hun voedsel. Voor hun is ijzer belangrijk voor het zuurstoftransport in hun lichaam. De hemoglobinegehalten in het bloed van zeewatervissen ligt vele male hoger dan dat in het bloed van zoogdieren zoals bijvoorbeeld de mens.
Het meten en toevoegen van IJzer
Voor we gaan toevoegen moeten we weten waarom we willen toevoegen, en hoeveel we willen toevoegen. Als ijzer een beperkende voedingstof kan zijn in de oceaan als er voldoende stikstof en fosfor aanwezig is, dan lijkt het logisch dat dit ook voor onze aquaria geldt, waar stikstof en fosfor in vele mate meer aanwezig is dan in de oceaan. Er is weinig bekend over ijzergehaltes in aquaria, En als er al een exact totaal (vrij en organische gebonden samen) ijzergehalte bekend zou zijn, dan kan men nog misleidt zijn als het ijzer niet in een biologisch beschikbare vorm aanwezig is (zoals in anorganische deeltjes of sterk gecheleerde organische moleculen). Het schijnt dat veel van de organische moleculen die ijzer binden in de natuur en in het aquarium aangemaakt worden. Als deze het ijzer te sterk binden, cheleren, is het ijzer niet biologisch beschikbaar. Het lijkt erop dat het dus zeer belangrijk is hoe het ijzer gebonden is. De totale hoeveelheid ijzer die we meten met testsetjes of ICP is dus waarschijnlijk niet zo relevant, omdat we eigenlijk geen idee hebben hoeveel van het ijzer biologisch beschikbaar is. Bij ijzer is er dus geen direct verband tussen concentratie en effect, zoals we dat wel zien bij bijvoorbeeld Calcium (Ca) of KH. Als u toch een test wil doen zijn merken zoals Tetra en Dupla en Mercks aan te raden.
Omdat het voedsel, wat we in het aquarium doen, grote hoeveelheden ijzer bevat, hoe verklaren we dan dat het water te weinig ijzer kan bevatten? Er zijn verschillende mogelijk belangrijke export mechanismes denkbaar voor aquaria. IJzer wat gebonden is aan organische moleculen kan afhankelijk van de aard van het organische molecuul snel worden afgeschuimd. IJzer wordt in het aquarium ook door veel organismen opgenomen. Ook kan het ijzer in het water soms gewoonweg niet biologisch beschikbaar zijn omdat het te sterk gebonden is aan bepaalde organische moleculen. Tenslotte kan ijzer ook gewoon neerslaan in het aquarium omdat de pH te hoog is. Het is zeker niet altijd nuttig ijzer toe te voegen. IJzer kan een bestaand algenprobleem (macro-algen, cyanobacteriën en micro-algen) versterken. In deze gevallen is het beter geen ijzer toe te voegen of op tijd te stoppen met toevoegen als de groei van micro-algen toeneemt. U kunt er van uitgaan dat als deze weelderig groeien, u geen ijzer tekort heeft.
Hoeveelheid toevoegen:
Het bepalen hoeveel ijzer je moet toevoegen is niet eenvoudig. Dit mede omdat we de waarde nog niet exact kunnen meten. Wel kunnen we observeren en aan bepaalde indicatoren zien of we een tekort hebben of we voldoende ijzer hebben. Overdosering van ijzer lijkt niet heel veel kwaad te kunnen. Toch moeten we het niet uitlokken en dit dan ook voorkomen. Het beste gebruik je een gerenommeerd A-merk om ijzer toe te voegen zoals Aqua-Medic, Salifert, Koralle-Zucht etc. Deze doseringen bevinden zich in veilige marges. Wil je toch zelf aan de slag? Ga dan eventueel aan de slag met het volgend recept. Ook hier geldt, alleen als je het net gelezen artikel goed begrijpt en vlot kunt doorlezen adviseren wij om dit recept te gebruiken. Weet waar je mee bezig bent, zoniet, blijf dan bij de merkproducten.
IJzer kun je toevoegen als oplossing:
Benodigdheden:
25 gram ijzersulfaat heptahydraat (FeSO4·7H2O)
250 ml water (H2O)
50,7 gram dinatriumcitraat (chelator) (E331(II)) (Na2H(C3H5O(COO)3))
Oplossing:
Neem exact 250 ml zuiver water (H2O) en voeg hieraan voorzichtig 50,7 gram dinatriumcitraat (Na2H(C3H5O(COO)3)aan toe. Vervolgens voeg je aan deze oplossing de 25 gram ijzersulfaat- heptahydraat (FeSO4·7H2O) toe. Deze oplossing komt uit op een totaal van 5 gram ijzer.
Dosering:
Voeg van deze oplossing 0,15 ml toe per 400 liter water per week. Met deze oplossing kom je ongeveer 5 jaar toe. Let op, de totale oplossing is goed om 3 miljard liter zeewater te verhogen van 0 ppm tot 0.000006 ppm!
De werkzame stof ijzersulfaat heptahydraat (FeSO4·7H2O) wordt ook wel melanteriet of ijzervitriool genoemd. Dit is een gehydrateerd ijzer(II)sulfaat (FeSO4). Het mineraal wordt gevonden in groene of blauwgroene stalactieten. De dinatriumcitraat is één van de drie zouten afkomstig van citroenzuur. Verwar dit niet met het zuur van een citroen, of citroenzuur zelf! Alle drie de zouten afkomstig van citroenzuur zijn in de Europese Unie toegelaten als voedingsadditief met als functie zuurteregelaar (voedingszuur).
Ook al ziet men over het algemeen weinig of geen effect van te veel ijzer toevoegen, is het goed te bedenken dat geen aquarium hetzelfde is, we hebben allemaal een verschillende, variërende bezetting. Als je vreemde, ongewenste reacties ziet, neem de dosering dan terug of stop er helemaal mee. Heb je besloten om met een gerenommeerd product te werken dan is het aan te bevelen ijzersupplementen te kopen waar het ijzer aan organische moleculen is gebonden. IJzer dat voor zoetwater verkocht wordt is vaak niet gebonden omdat ijzer beter oplosbaar is bij de lage pH’s van zoetwateraquaria. Het is beter deze producten niet in het zeewateraquarium te gebruiken. Als het goed is gebruiken de fabrikanten geen organische moleculen die het ijzer te sterk binden, maar stoffen als EDTA en citraat, die fotochemisch degraderen en continue een beetje ijzer vrij geven.
Een andere manier om ijzer toe te voegen is door middel van fosfaatverwijderaars. Dit kan door middel van gekochte korrels ijzer(III)oxide (Fe2O3) maar ook door vloeibare ijzer(III)chloride (FeCl3) die een vlokreactie veroorzaakt. Toch raad ik u deze laatste methode niet aan net zoals het gebruik van lantaan (La). Lantaan (La) reageert onmiddellijk met stikstof en alle halogenen. Dit is dus niet gewenst. Later zullen we in een ander artikel dieper ingaan op fosfaatverwijderaars.
Het is en blijft een beetje experimenteren. IJzer is een element dat niet veel kwaad kan zolang je maar goed in de gaten houd wat er met uw aquarium gebeurd. Mistig water, en overdadige algengroei is vaak een teken van een te hoge waarde. Onthoud dat als ijzer te weinig aanwezig is, het toevoegen ervan kan helpen. Maar als het al beschikbaar was dan was het toevoegen ervan zinloos en in sommige gevallen zelfs gevaarlijk. Wanneer u start met toevoegen moet u observeren. Ziet u na twee weken geen verschil kunt u dus stoppen, het ijzergehalte was en is dan goed.
Waar op te letten bij toevoegen:
een paar zaken waar je op moet letten als je ijzer toevoegt.
Ü Sommige publicaties wijzen erop dat cyanobacteriën ook in situaties met weinig ijzer goed gedijen. Dit zou onder andere komen omdat ze stoffen maken die ijzer (in water) goed binden. Dit geeft ze een competitief voordeel ten opzichte van andere organismes die ook ijzer nodig hebben. Het is voor aquarianen echter wel verstandig hier op te letten en de ijzertoevoeging te stoppen als je cyanobacteriën (rode flap) ziet opkomen.
Ü Naast zoöxanthellen en cyanobacteriën kunnen ook diatomeeën sneller gaan groeien. In het kweekmilieu is men hier gelukkig mee, in het aquarium zijn ze vaak ongewenst (uit esthetisch oogpunt). Wel is het zo dat door een goed ijzergehalte fotosynthetische dinoflagellaten zullen afnemen omdat de andere organismen beter tegen hen kunnen concurreren. Wanneer er een overschot aan ijzer is moet je opletten dat macro-algen niet extreem gaan groeien. IJzer blijft immers een soort algenmest. Wanneer u werkt met synthetisch zeewater moet u ook opletten. In de meeste merken zout zit ijzer (als ballast) t.o.v. natuurlijk zeewater.
Ü Ook kan ijzer tegengewerkt worden door andere elementen en waarden. wanneer er fosfor en fosfaten aanwezig zijn zullen onze zoöxanthellen moeilijk ijzer kunnen opnemen. Dit is een van de redenen dat fosfaat ongewenst is! Maar ook omgekeerd, ijzer remt de opname van fosfor. Twee elementen die continu in gevecht zijn met elkaar. Het toevoegen van bijvoorbeeld ijzer(III)oxide (Fe2O3) zorgt voor fosfaatdaling. Hoge calciumwaarden (Ca) remmen ook de opname van ijzer net zoals die van Mangaan (Mn) en fosfor. Calciumwaarden houdt u dan ook best tot maximum 430. Ook moeten we opletten wanneer we kalkwater, calciumhydroxide (Ca(OH)2), toevoegen. De hoge pH kan ervoor zorgen dat het toegevoegde ijzer meteen neerslaat. voor vissen is ijzer relatief onschadelijk. Er zijn meldingen dat gele dokters (Zebrasoma flavescens) slecht reageren op bepaalde ijzertoevoegingen. Toch zijn hier geen echte bewijzen of onderzoeken van bekend.
Wat effect heeft IJzer op ons systeem? Soortspecifiek
Effect van ijzer op het koraal Stylophora pistillata
In tegenstelling tot het onderzoek in oceanen is er nog weinig onderzoek gedaan naar het effect van ijzer in aquaria. Een van de belangrijkste onderzoeken is het onderzoek van Ferrier-Pages. (Response of a scleractinian coral, Stylophora pistillata, to iron and nitrate enrichment). Hier hebben ze koraalstekken in verschillende bakken gezet waar ze Middellandse Zeewater door leidden. Het water werd steeds chemisch veranderd, waarbij men steeds de koraalgroei, de zoöxanthellendichtheid, fotosynthesesnelheid en de chlorofylhoeveelheid bekeek. Het Middellandse Zeewater bevatte heel weinig voedingsstoffen (nitraat< 0.06 ppm, fosfaat <0.02 ppm, ijzer < 0.2 ppb). Voor de test werd het ijzer verhoogd naar 0,3 ppb, nitraat naar 0.15 ppm. Waarden die veel lager zijn dan in de meeste aquaria. Het water werd zo snel rondgepompt dat ieder uur een aquariumvolume ververst werd.
Als we eerst eens naar de zoöxanthellendichtheid kijken. Deze dichtheid is een maat voor de hoeveelheid zoöxanthellen die aanwezig zijn. Door het verhogen van het ijzer- en nitraatgehalte werden de hoeveelheden zoöxanthellen behoorlijk vergroot in vergelijk met de controlekoralen. De grootste toename werd gemeten als er alleen ijzer toegevoegd werd. Hetzelfde geldt voor het chlorofylgehalte. Het lijkt er dus op dat de zoöxanthellengroei beperkt werd door ijzer en nitraat, en dan vooral ijzer. Later zullen we nog bespreken of deze zoöxanthellengroei gewenst is en of deze groei ook langer doorgaat dan de drie testweken. De onderzoekers hebben ook verschillende aspecten van fotosynthese gemeten voor deze koralen. Ze vonden dat de fotosynthese in alle gevallen toenam met de grootste stijging als er alleen ijzer toegevoegd werd. Echter, als er rekening werd gehouden met de toename van de zoöxanthellen werd er per zoöxanthel niet meer geproduceerd. De toegevoegde nutriënten hadden blijkbaar alleen effect op de hoeveelheid zoöxanthellen en niet op de fotosyntheseactiviteit.
Tenslotte hebben ze ook de koraalgroei gemeten door de stukken te wegen. Het bleek dat de groeisnelheid behoorlijk was afgenomen. Zowel ijzer als nitraat en combinaties hiervan veroorzaakte een groeiafname van wel 30%. Het lijkt erop dat ijzer en nitraat giftig zijn voor de koralen ondanks dat de hoeveelheid zoöxanthellen toeneemt. De aard van deze “giftigheid” is waarschijnlijk minder ernstig voor aquarianen dan het in eerste instantie klinkt. De onderzoekers denken dat de snelle zoöxanthellengroei toch niet veel waardevolle producten levert voor het koraal, en dat vandaar de groeisnelheid afneemt. Ze benadrukken wel dat het verband tussen calcificatie en ijzer toevoegen onduidelijk blijft.
Ook hier weer de vraag of dit een tijdelijk effect is of dat dit langere tijd doorgaat. Alleen lange duurexperimenten kunnen hier een antwoord op geven. Een andere verklaring zou een tekort aan fosfaat kunnen zijn. Bij micro-algen is fosforlimitatie vaak minder belangrijk dan stikstoflimitatie. In de oceaan is het nitraat meestal eerder verbruikt voordat het fosfaatgehalte te laag is. Het is echter best wel mogelijk dat koralen te weinig fosfaat krijgen bij deze lage concentraties zoals in deze test gebruikt, vooral als ze extra nitraat krijgen. Het zou dus mogelijk kunnen zijn dat door de snelle zoöxanthellengroei alle fosfaat opgebruikt is en er geen fosfaat meer beschikbaar is voor koraalgroei. Het is wel duidelijk dat het niet zo eenvoudig is om de testresultaten te gebruiken voor aquaria, maar het geeft wel een indicatie waar we op moeten letten, en wat mogelijke ingrepen zijn.
Effect van ijzer op overige koralen en koraalkleuren
Als er een toename van zoöxanthellen optreed, is het mogelijk dat de mooi gekleurde koralen donkerder van kleur worden. Een toename heeft vaak als oorzaak dat de reeds bestaande zoöxanthellen niet alleen in staat zijn om in de voedingsbehoefte te voorzien. De zoöxanthellen zijn dus gezond en zelf in staat om te vermeerderen. Het donkerder worden van de koralen kan dus wijzen op genoeg aanwezig en beschikbaar ijzer. Gele koralen, in het bijzonder Acropora sp., kunnen erop wijzen dat als ze groen worden ze teveel ijzer tot hun beschikking hebben. Ook wanneer er te weinig ijzer is kun je dit bij sommige koralen zien. Rode Acropora sp. zoals Acropora hyacynthushebben een ijzertekort wanneer ze langzaam roze beginnen te worden. Ook wanneer groene Acropora sp., zoals Acropora yonghei, lichter beginnen te worden en zelf naar het gele toe neigen kunt u er vanuit gaan dat u te weinig ijzer heeft. Heliopora coerulea ook wel blauwkoraal is geen steenkoraal maar heeft toch een skelet. Dit is een pareltje uit de evolutie. Het teveel opgenomen ijzer slaat het koraal op in ijzerzout (ijzer(II)sulfaat (FeSO4)) en calciumcarbonaat (CaCO3). Zo vormt het typisch blauwe skelet. Vaak kun je aan een Heliopora sp. zien of het ijzergehalte te laag is. Wanneer de groeitoppen snel verpulveren of zeer broos zijn is er een ijzer tekort. Jammer genoeg is het een ondergewaardeerd koraal wat in weinig aquaria terug te vinden is.
Gids voor het kleuren van SPS koralen
Gids voor de kleuring van SPS koralen
Onlangs las ik een post van Ryan Gripp op de website www.reefbuilders.com over het verband tussen de toevoegingen van sporenelementen en de kleuring van SPS koralen. Ik kon het niet nalaten om u te laten meegenieten van deze ervaringen en vertaalde de forumpost.
Deze gids poogt om u te helpen bij het kweken van SPS koraal. Dit werd geschreven door het forumlid Shadowramy en het verduidelijkt specifieke ideeën en strategieën waarmee u de kleur van uw SPS koralen kan beïnvloeden. Dit veronderstelt dat u een min of meer fundamenteel inzicht hebt in de waterparameters in uw aquarium. In het verleden werd ik vaak gevraagd een artikel over koraalkleuring te schrijven evenals mijn eigen ervaringen over specifieke methodes voor het bereiken van bepaalde kleuren. Gewoonlijk vraagt men mij: “Hoe krijgt u goede kleuren?” Dan antwoord ik met de vraag: “Welke specifieke kleur wil u verbeteren?” In de loop van de afgelopen verscheidene maanden heb ik gewerkt aan methodes om bepaalde kleuren te krijgen. Ik heb eigen testen gedaan evenals heel wat andere aquaria bezocht en gezien wat zij deden om bepaalde kleuren te verkrijgen. Ik denk dat ik nu definitief een basisgids heb gemaakt voor zij die het interessant vinden.
Gelieve er nota van te nemen dat ik veronderstel dat u aan de minimum vastgestelde normen voldoet voor het houden van SPS koralen, namelijk sterke verlichting, het juiste calciumgehalte, een sterke eiwitafschuimer en levend steen.
Gele SPS koralen
Is erg afhankelijk van het nitraat- en fosfaatgehalte. Alle SPS kleuren zijn erg afhankelijk van een gebrek aan N en P maar ik wil met de gemakkelijkst te verkrijgen kleur beginnen, namelijk geel.

De gele koralen zijn een soort barometer; de gele koralen zullen u het eerst waarschuwen over wat in uw aquarium gebeurt, wat nodig is en wat over gedoseerd is. Nitraat (NO3) en/of fosfaat (PO4) verminderen is het belangrijkst, ofwel door technische middelen zoals nitraat- en fosfaat reductiemiddelen of biologisch door Deep Sand Bed (DSB), het inzetten van actieve koolstof en/of waterverversingen.
Als u SPS koralen wilt kweken, zou ik voorstellen dat u begint met een Acropora die geel is.
Als u er kunt in slagen om ze gedurende verscheidene maanden geel te houden, dan zou u klaar moeten zijn om andere kleuren te houden.
Groene SPS koralen
Groen zou de volgende gemakkelijkste kleur zijn. De meeste groene kleuring kan door de toevoeging van een ijzerconcentraat worden bereikt. U moet met ijzer zeer zorgvuldig zijn omdat het ook een voedingsstof voor algen is. Vandaar dat het zo belangrijk is om eerst uw gele kleuren op punt te zetten (dus eerst uw N en P verminderden). Bovendien, gebruik ik mijn gele koralen als indicatoren voor mijn groene en blauwe koralen.
Als uw groene koralen een bruine kleur krijgen of zij verbleken dan is dat waarschijnlijk te wijten aan een gebrek aan ijzer. U kan ijzer bijvoegen tot u vermeerdering van de algengroei vaststelt of tot uw gele Acroporas een groene flikkering vertonen (het zal geen hevig groen zijn maar een groen/gele schijn zijn).

Als het weefsel donkerder wordt dan hebt u teveel ijzer toegevoegd. Een ander teken van overdosering is de groei van algen. Indien nodig beëindig dan onmiddellijk de toevoeging van ijzer en een waterverversing kan ook het teveel aan ijzer verminderen.
Zoals met alles in onze rifaquaria moet elke verandering langzaamaan gebeuren.
Blauwe en sommige purperen SPS koralen
Dit is hoofdzakelijk voor blauwe koralen maar ik heb ondervonden dat het ook effect kan hebben op de purperen koralen. Het toe te voegen supplement is een kalium-jodide-oplossing, ook Lugol-oplossing genoemd.

Men begint met doseren wanneer de blauwe kleuren minder intens worden. Opnieuw, gebruikmakend van de gele koralen als indicatoren, stopt men met doseren wanneer de gele koralen een groene schijn vertonen.
Rode/Roze en sommige purperen SPS koralen
Hoofdzakelijk voor het kleuren rood en roze in Montiporas, Styloporas, Pocilloporas en Seriatoporas. Het supplement is kalium (niet kaliumjodide). Als u een hoge kalium zoutmengeling zoals Oceanic, Tropical Marine Pro gebruikt en u regelmatige waterveranderingen doet, dan gaat u dit waarschijnlijk niet veel moeten aanvullen.

Voor het doseren kunt u uw Monitporas als indicatoren gebruiken. Aanvullen is vereist wanneer de Montiporas langzamer groeien en de groeiranden een grijze schijn vertonen. Wanneer de Styloporas en Pocillopoeras lijken alsof zij aan de lucht blootgesteld zijn, dan is dat een indicator van kaliumgebrek. De poliepen zijn dan volledig teruggetrokken en de kleuren zijn licht. Andere indicatoren van kaliumgebrek is wanneer roze koralen lichtbruin kleuren en wanneer Acroporas hun kleur verliezen en lichter of bleker worden. Een belangrijk kaliumgebrek doet het weefsel van de koralen lossen, meestal beginnend van de basis en zo naar de toppen toe.
Een overdosis kan leiden tot het verbranden van de tippen. Opgelet, niet te verwarren met nieuwe groei. De brandwonden van de uiteinden zullen wit zijn zonder poliepen.
Purperen SPS koralen
Vanuit mijn ervaring waarschijnlijk één van de moeilijkste kleuren van alle Acroporas aangezien het een combinatie van verscheidene variabelen is.
Eerst en vooral is er de waterhelderheid, wat betekent dat men over actieve koolstof of een ander verhelderend medium dient te filteren. Met biologische filters kan ook de gewenste helderheid bekomen worden, zoals Zeoviet. Ook sponsen en Tridacna’s filteren het water.

Verhoogde waterhelderheid zal eerst de uiteinden van de SPS koralen beter kleuren, maar niet de volledige basis. Ik heb nana en valida met werkelijk mooie purperen uiteinden gezien, maar met bruingebleekte, witte basissen. Ik heb dezelfde nana en valida in het aquarium van iemand anders gezien, die alle andere parameters goed hadden met volledig purper van de basis tot aan het uiteinde van de koralen.
Het tweede belangrijkste punt is de verlichting. Van mijn observaties van mijn eigen en andere aquaria, houden purperen koralen van 420 tot 440nm uit het lichtspectrum, Deze kleuren komen voor in actinic-lampen en 20K halogeniden. De mooiste purperen koralen die ik zijn in aquaria heb gezien stonden onder 440nm blauwe actinics (ATI Blue+, Giesemann Actinic) of 20K Halogeniden (Radium, XM 20K).
Ten derde, supplementen zoals jodium en kalium (zie blauw en Rood/Roze). Opnieuw, zorg ervoor uw groene koralen groen zijn en de gele koralen geel zijn. Uw blauw zou helder met diepte moeten zijn. Het jodide zal ook helpen als u uiteinde-brandwonden hebt.
Dit zijn enkel mijn observaties en testervaringen en ik ben er zeker van dat in de toekomst andere factoren en toevoegingen zullen worden gevonden.
De manier waarop je deze toevoegingen kan bereiden kan je vinden op de website www.reefsecrets.org tabblad artikel categoriën, dan tabblad zeewater aquarium chemie, dan tabblad Publicaties, dan artikel “Balling methode: Toevoegingen aan het zeeaquarium” of rechtstreeks via deze link /https://www.reefsecrets.org/index.php/chemie/chemie-publicaties/balling-methode-toevoegingen-aan-het-zeeaquarium
















